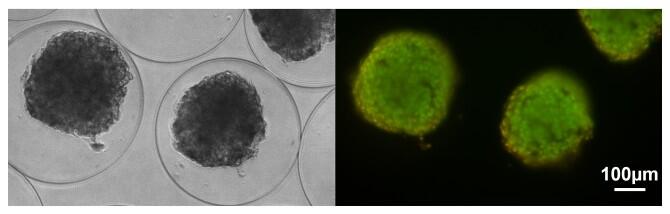
La diabetes mellitus tipo 1 (DMT1) contribuye al 10 % del total de casos de diabetes mellitus en todo el mundo, principalmente en personas jóvenes, y se considera un peligro para la salud en aumento. DMT1 se caracteriza por una destrucción autoinmune de las células del páncreas que producen insulina (islotes pancreáticos), que resulta en una deficiencia severa de insulina y, posteriormente, la elevación de los niveles de glucosa en la sangre. Actualmente, la terapia basada en inyecciones de insulina es el tratamiento que se aplica en pacientes diabéticos tipo 1. Sin embargo, además de las complicaciones médicas que supone a largo plazo, este tratamiento requiere múltiples mediciones diarias de glucosa en sangre y administración de insulina subcutánea en los pacientes por el resto de sus vidas.
Alternativamente, “el trasplante de islotes pancreáticos aislados del páncreas de donantes proporciona una nueva fuente de células productoras de insulina capaces de aportar los requerimientos de insulina acorde a los niveles de glucosa en la sangre en pacientes con DMT1. Uno de los obstáculos del trasplante de islotes es el uso a largo plazo de inmunosupresores para evitar el rechazo inmune de los islotes trasplantados, los cuales reducen las defensas del paciente e implican complicaciones médicas severas”, explica el autor del trabajo Albert Espona Noguera. “Para evitar este problema —continúa—, los islotes pancreáticos pueden aislarse del sistema inmune del paciente mediante técnicas de microencapsulación donde los islotes son encapsulados en microcápsulas hechas de materiales biocompatibles (no tóxicos). Entre muchos materiales utilizados en la microencapsulación de células, el alginato es el material más utilizado. Este polímero natural tiene excelentes propiedades para aplicaciones biomédicas ya que ofrece una alta biocompatibilidad y una baja toxicidad”. Sin embargo, “la técnica de microencapsulación tiene varios obstáculos técnicos que dificultan su aplicación clínica. Un problema crucial es el alto número de microcápsulas vacías generadas durante el proceso de microencapsulación de los islotes, lo que lleva a un gran incremento del volumen de microcápsulas a implantar, que puede aumentar la reacción inmunitaria del huésped después de la implantación” comenta Espona Noguera.
Con el fin de evitar el elevado número de microcápsulas vacías, “hemos propuesto un enfoque novedoso para la purificación de islotes microencapsulados para reducir el volumen del implante separando los islotes microencapsulados de las microcápsulas vacías”, explica el investigador de la UPV/EHU-Ciber BNN que forma parte de la ICTS (Infraestructura Científico-Técnica Singular) de Nanbiosis. “Hemos desarrollado un sistema de separación magnética de microcápsulas que combina distintas tecnologías: nanopartículas magnéticas y un chip microfluídico, es decir, un chip con canales de tamaño micrométrico, obtenido mediante técnicas de impresión 3D que contiene imanes posicionados estratégicamente”, añade el investigador. “Para la separación de las microcápsulas, los islotes pancreáticos son puestos en contacto con las nanopartículas magnéticas, confiriéndoles así propiedades magnéticas.
Después los islotes son microencapsulados, obteniendo de esta manera cápsulas conteniendo los islotes magnéticos y cápsulas vacías no magnéticas. Cuando las microcápsulas son bombeadas a través de los microcanales del chip, los imanes desplazan las cápsulas magnéticas hacia un microcanal de salida, mientras que las cápsulas vacías no magnéticas siguen su curso por otro microcanal de salida”, detalla. De esta manera, “conseguimos eliminar las cápsulas vacías y, en consecuencia, reducimos el volumen de implante terapéutico de microcápsulas. La gran eficiencia de purificación de este sistema de separación magnética nos ha permitido reducir el volumen de implante casi un 80 %, reduciendo así las complicaciones derivadas de la implantación de grandes volúmenes de microcápsulas y proporcionándonos una nueva alternativa para el tratamiento de la DMT1”, subraya Espona Noguera.
Además, “en este trabajo hemos estudiado la funcionalidad de los implantes purificados en modelos animales diabéticos. Hemos observado que después de la implantación subcutánea de los islotes microencapsulados en animales diabéticos, los niveles de glucosa en sangre se restablecieron en los niveles normales durante casi 17 semanas” añade. (Fuente: UPV/EHU)